Водород – это необычайно легкий газ – он в 14 раз легче воздуха и в два раза легче гелия. Если надуть им резиновый шарик, он взлетит ввысь. Это свойство водорода использовали раньше для наполнения воздушных шаров и дирижаблей. Сегодня мы будем получать водород химическим способом из легкодоступных материалов и заставим шарик летать. Мы изучили несколько способов получения водорода при помощи химической реакции. При выборе мы исходили из наличия доступных реактивов и безопасности. И самый простой способ получить водород в домашних условиях – это реакция алюминия, медного купороса и пищевой соли в воде (Al+CuSO4+NaCl+H2O). Для эксперимента нам понадобилось следующее оборудование: бутылка пластиковая 1л, капельница (продается в любой аптеке за копейки), медный купорос (в хоз-товарах в отделе удобрения для растений), пищевая соль, алюминиевая пищевая фольга (или алюминиевая проволока), надувной шарик. Подготовительные работы: В пробке от пластиковой бутылки нагретым на плите гвоздем проделываем отверстие. В это отверстие вставляем пластиковый соединитель от капельницы и приклеиваем (мы использовали супер-клей). Затем на этот соединитель надеваем трубку капельницы. Толстый конец капельницы обрезаем, как показано на рисунке. На него мы надеваем резиновый шарик. 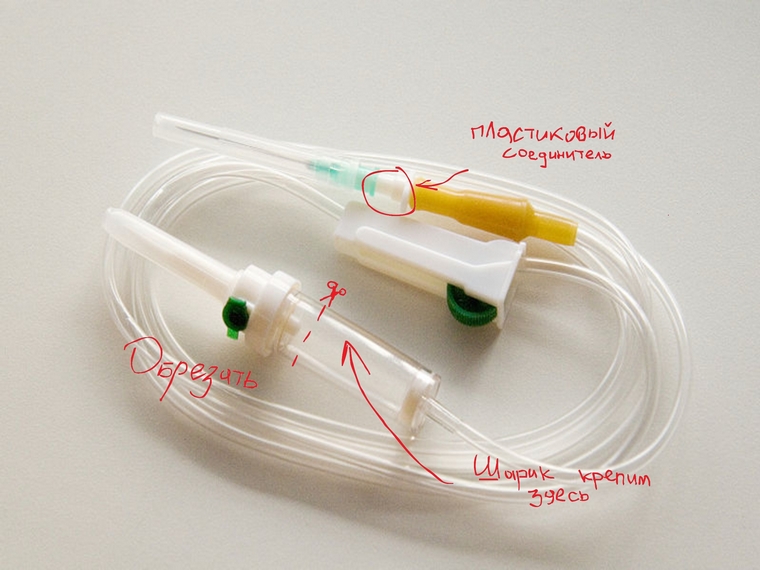
Ход эксперимента. В литровую пластиковую бутылку насыпали равное количество медного купороса и пищевой соли (по 100г, соли можно больше). Затем залили водой (примерно 700 мл) и взболтали до полного растворения. Раствор окрасился в ярко зеленый цвет. Далее необходимо заготовить алюминиевые комочки из пищевой фольги (такие по размеру, чтобы легко и быстро проходили в горлышко бутылки) . Если есть алюминиевая проволока, используйте ее (метра два алюминиевой проволоки сложите зигзагом, чтобы получился пучок легко пролезающий в бутылку). Мы использовали и то ,и другое. Бутылку с раствором медного купороса и соли нужно поставить предварительно в емкость с водой (кастрюля или ведерко). Так как в ходе реакции бутылка будет сильно нагреваться и может расплавиться. (Также раствор может быстро закипеть без охлаждения и выскочить наружу прежде, чем Вы закроете пробку. Проверено!). Затем нужно закинуть в бутылку проволоку и фольгу и закрыть подготовленной крышкой с трубкой. Делать это нужно быстро, так как реакция начинается мгновенно и водород начинает выделяться сразу. Результат: Мы наблюдем, как образуется множество пузырьков водорода около алюминия. Над поверхностью раствора виден белый дымок пара. При реакции выделяется большое количество тепла и наша бутылка сильно нагревается. Со временем цвет раствора меняется на более темный, а затем и вовсе становится черным. Комочки алюминия окрашиваются в ржаво-оранжевый цвет. Это на них выделяется медь из раствора медного купороса. Через отверстие в пробке по трубке водород поступает в шарик. Шарик постепенно наполняется водородом и через 10-20 минут реакции уже видно, как он поднимается в воздух. Примечание: для того, чтобы шарик проще надувался водородом следует до начала эксперимента его растянуть, т.е. надуть несколько раз и сдуть. Смотрите видео эксперимента...
Как это работает (Химическая реакция): Алюминий – активный металл. В чистом виде он вступает в химическую реакцию с водой, растворяясь в ней, при этом выделяется водород. Но, если бросить алюминий в воду, никакой реакции не наблюдается. Почему?! А все потому, что алюминий защищен оксидной пленкой. Чтобы реакция началась нужно разрушить эту пленку. Под действием медного купороса (CuSO4) + пищевой соли (NaCl) эта оксидная плёнка разрушается, а алюминий реагирует с водой с образованием водорода H2 и гидроокиси алюминия Al(OH)3. 1) CuSO4 + 4NaCl<=> Na2[CuCl4] + Na2SO4 Медный купорос и хлорид натрия образуют комплекс. Раствор становится ярко зеленого цвета. Происходит реакция алюминия с водой с выделением водорода (H2). | |
| Просмотров: 20619 | | |